Klaus U. Meier, Richard Reichl
Hinter dieser Frage steht die Hoffnung und der Wunsch, dass auf Tierversuche in der experimentellen Forschung bereits heute oder aber in absehbarer Zeit verzichtet werden kann. Diese Hoffnung wird getragen von dem Wunsch, Tieren Leiden und Schmerzen zu ersparen. Hierbei darf aber nicht vergessen werden, dass Tiere von Menschen für unterschiedlichste Zwecke genutzt werden: Als Nahrungs- und Rohstofflieferant, als Arbeits- und Heimtier, zu Sportzwecken und auch als Versuchstier.
Bei all diesen Formen der Tiernutzung stellt sich die Frage nach den Belastungen, unter denen diesen Tieren Leistungen abverlangt werden. Im Besonderen bei Tieren im Experiment wird eine hohe Belastung angenommen. Hieraus wird ein erhöhtes Schutzbedürfnis für diese Tiere abgeleitet.
Der Schutz von Mensch, Tier und Umwelt vor möglichen Gefährdungen durch Chemikalien ist oberstes Gebot für die Industrie. Der Verbraucher und die Bevölkerung erwarten, dass die Industrie im Rahmen der Verantwortung für die Sicherheit ihrer Produkte alles unternimmt, um mögliche Gefährdungen rechtzeitig zu erkennen. Der Gesetzgeber fordert durch entsprechende Verordnungen und Vorschriften die Durchführung entsprechender experimenteller Untersuchungen, die bei Zulassung der Produkte in Form von Prüfberichten und daraus resultierenden Bewertungen erbracht werden müssen.
Zur Erfüllung dieser Aufgaben wird in der experimentellen biomedizinischen Forschung eine breite Palette von Untersuchungsmethoden eingesetzt. Ein Großteil davon sind Tierversuche. Daraus kann sich ein Konflikt mit der ethischen Norm ergeben, nach der der Mensch aus Verantwortung für das Tier als Mitgeschöpf dessen Leben und Wohlbefinden zu schützen hat und ihm ohne vernünftigen Grund keine Schmerzen, Leiden oder Schäden zufügen darf (§ 1 Tierschutzgesetz).
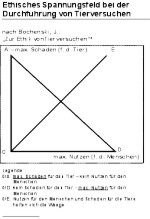
Mit dieser Situation muss sich der Experimentator täglich aufs Neue auseinandersetzen: Mit seinem Tierversuch möchte er einen maximalen Erkenntnisgewinn und damit größtmöglichen Nutzen für den Menschen erzielen. Demgegenüber steht der eventuelle Schaden für das Versuchstier, sofern sich kein oder nur ein geringer Nutzen für den Menschen ableiten lässt (Abb.1).
Eine solche Abwägung dieser beiden ethischen Prinzipien entfällt allerdings beim Einsatz von „Alternativmethoden“ (besser: EuE = Ersatz- und Ergänzungsmethoden zu Tierversuchen). So wird verständlich, dass der Ruf nach „Alternativmethoden“ immer lauter wird, wobei zu berücksichtigen ist, dass diese Methoden für viele Fragestellungen ungeeignet sind.
Hierzu bedarf es der exakten Definition des Begriffes „Alternativmethode“: Dies sind Versuchsanordnungen, bei denen der lebende Organismus durch schmerzfreie Materie ersetzt wird, ohne dass die Aussagekraft des Experimentes am Tier (als Gesamt- organismus) geschmälert wird. Im weiteren Sinne sind damit auch Versuchsanordnungen gemeint, die die Belastung der Versuchstiere reduzieren oder auf sog. „niedrigere“ Tierarten ausweichen. Hier werden im Besonderen die von Russel und Burch bereits 1959 erhobenen Forderungen der „3 R‘s“ berücksichtigt:
„REPLACE“: Ersatz von Versuchen am lebenden Tier durch andere Methoden
„REDUCTION“: Verringerung der Anzahl der eingesetzten Versuchstiere
„REFINEMENT“: Verminderung der Belastung der Versuchstiere im Versuch durch Verfeinerung der Methoden
Unter dem Überbegriff „in-vitro-Testsysteme“ versteht man Untersuchungen in „schmerzfreien“ Systemen. Diese sind nur teilweise Ersatzsysteme zum eigentlichen Tierversuch. Häufiger aber ergänzen diese methodischen Ansätze den Tierversuch, z. B. bei der Aufklärung des toxikologischen Wirkungsmechanismus, schließen aber den Einsatz tierexperimenteller Versuchsreihen nicht aus.
Auf der Basis des Arzneimittel-, Chemikalien- und Pflanzenschutzgesetzes müssen die Stoffe aufgrund ihrer toxikologischen Eigenschaften eingestuft und gekennzeichnet werden. Die hierfür erforderlichen Untersuchungen sind also vom Gesetzgeber vorgeschrieben. Die geforderten Daten lassen sich – von wenigen Ausnahmen abgesehen – nur aus Tierversuchen verifizieren. Die Verantwortung für eine sachgerechte Gefährdungsbeurteilung hierfür liegt allein beim Hersteller und demjenigen, der die Substanzen in Verkehr bringt. Er allein ist dafür haftbar, dass sein Produkt auf der Basis des aktuellen wissenschaftlichen Kenntnisstandes geprüft wird, was von der Behörde im Rahmen des Anmeldungs- oder Zulassungsverfahrens überprüft wird.
Nach SPIELMANN haben in-vitro-Methoden sicherlich einen hohen Stellenwert, aber häufig ist die Aussagefähigkeit dieser Untersuchungen in der Toxikologie begrenzt. Einige Aspekte sind als Vorteile hervorzuheben:
– Arbeiten unter kontrollierten Versuchsbedingungen bei gleichzeitiger Ausschaltung systemischer Einflüsse
– Prüfung an einer grossen Zahl von Testsystemen möglich
– Geringe Mengen an Prüfsubstanz erforderlich
– Einsatz bei der Vorprüfung von Pharma-Entwicklungsprodukten
– Aufklärung des Wirkungsmechanismus
– Möglichkeit des Einsatzes von menschlichen Zellen und Geweben
Gerade der letzte Punkt ermöglicht die Untersuchung und evtl. Beantwortung wissenschaftlicher Fragestellungen, die aus ethischen Gründen nicht an menschlichen Probanden durchgeführt werden können.
Neben Aspekten der Ethik und des Tierschutzes gibt es für die forschende chemisch-pharmazeutische Industrie weitere wichtige Gründe zum Einsatz von EuE-Methoden:
– Tierversuche dauern lange, sind aufwendig und damit kostenintensiv
– Personelle und materielle Ressourcen werden über große Zeiträume gebunden
Ein Grund mehr für den Forscher, die meist auch kostengünstigeren Ersatzmethoden einzusetzen. Die Nachteile von in-vitro-Testsystemen dürfen dabei aber nicht übersehen werden:
– Keine Erfassung systemischer Einflüsse, vor allem der Wechselwirkungen zwischen den verschiedenen Organsystemen
– Unzureichende bis keine Erfassung organspezifischer Effekte
– Keine Erfassung komplexer toxischer Wirkungen wie in der Reproduktionstoxikologie und Kanzerogenitätsprüfung
-Keine Erfassung chronischer Effekte
– Keine Erfassung der Reversibilität oder Heilung toxischer Effekte
– Keine Erfassung von Empfindungen (wie z. B. Schmerz)
– Keine Erfassung der Interaktionen zwischen verschiedenen Geweben, Organen und Organsystemen
– Unzureichende Berücksichtigung pharmakokinetischer und metabolischer Aspekte
Von wenigen Ausnahmen abgesehen (z. B. Ames-Test):
– Keine behördliche Akzeptanz bei der sicherheitstoxikologischen Bewertung von Arzneimitteln
– Keine behördliche Akzeptanz für die toxikologische Einstufung und Kennzeichnung chemischer Stoffe und Zubereitungen.
In dem Maß, in dem Ersatzmethoden zum Tierversuch von den Zulassungsbehörden akzeptiert werden, wird sich auch die Zahl der eingesetzten Versuchstiere verringern (Abb. 2).
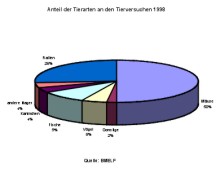
Der Anteil der einzelnen Tierarten, die zu Tierversuchen herangezogen werden veranschaulicht die Abbildung 3.

Das Diagramm zeigt, daß der überwiegende Anteil der verwendeten Versuchstiere Mäuse und Ratten sind (76%). Die Zahl von 2% für „Sonstige“ beinhaltet die großen Versuchstiere wie Primaten (keine Menschenaffen), Schweine, Hunde und Katzen. Da ist ein drastischer und somit sehr erfreulicher Rückgang gegenüber den achtziger und Anfang neunziger Jahre zu verzeichnen.
In den nachfolgenden Jahren (1999-2001) hat sich an dieser Verteilung kaum etwas geändert.
Die Abbildung 4 zeigt die Verteilung der Versuchstiere nach ihrem Verwendungszweck, was eindrucksvoll belegt, daß rund 90% der verwendeten Versuchstiere der Prüfung neuer Arzneimittel der Grundlagenforschung und der Erforschung neuer medizinischer Behandlungsmethoden des Menschen dienen.

Auf dem Arbeitsgebiet der Gentoxizität gibt es eine Vielzahl von in-vitro-Testmethoden zur Bewertung der verschiedenen genetischen Endpunkte. Die Zahl der routinemäßig durchgeführten und seitens der Behörden akzeptierten Methoden ist jedoch gering. Hier zeigen sich auch die Schwierigkeiten und Vorbedingungen bei der Realisierung von Ersatzmethoden zum Tierversuch, die allerdings auch für die Einführung neuer tierexperimenteller Prüfmethoden gelten sollten:
– Die Ergebnisse aus diesen Methoden müssen – wie bei in-vivo-Versuchen auch – reproduzierbar sein und
– die Aussageschärfe der neuen Methoden muss auf Basis einer breiten Palette an Referenzsubstanzen validiert und auf internationaler Basis seitens der Behörden akzeptiert sein.
Im Bereich der Toxikologie gibt es inzwischen einige Methoden, die entweder mit einer deutlich geringeren Tierzahl pro Versuchsansatz genügend Informationen erbringen oder gänzlich auf den Versuchstiereinsatz verzichten: Hier ist die ATC-Methode (Acute Toxic Class Method) mit einem deutlich geringeren Versuchstiereinsatz zu nennen; diese Methode wurde 1994 von der OECD akzeptiert. Als versuchstierfreie Methode ist der HET-CAM-Test (Hen Egg Test – Chorion Allantoic Membrane) aufzuführen, der zumindest bei stark reizenden Stoffen zu einer Übereinstimmung mit den Ergebnissen aus dem umstrittenen DRAIZE-Test (Primäre Reizwirkung am Auge bzw. an der Haut nach John Draize (1944)) führt.
Mit in-vitro-Methoden können heute durchaus erste Erkenntnisse zur Wirkungsweise und zum Wirkungsmechnismus einer Chemikalie erzielt werden. Andere Fragestellungen, wie z. B. komplexe Wechselwirkungen zwischen den verschiedenen Organsystemen oder eine Wirkung im wachsenden Organismus mit seinen vielfältigen Funktionen, lassen sich aber derzeit auch weiterhin nur an einem intakten Säugerorganismus prüfen. Für den Versuchsleiter gilt dabei der Grundsatz: so viel an Versuchen wie nötig, aber auch so wenig wie möglich.
Gerade bei der toxikologischen Risikoabschätzung für den Menschen wird man daher bis auf Weiteres auf Tierversuche nicht verzichten können, wobei jedoch die gesamten Bemühungen darauf ausgerichtet sind. Dies wird unterstrichen durch die Aussage der früheren Bundesgesundheitsministerin Frau Andrea Fischer: „Solange wir auf Tierversuche noch nicht verzichten können, weil wir sie brauchen, um die Gesundheit des Menschen zu schützen, solange haben wir die ethische Pflicht, nach alternativen Testverfahren an schmerzfreier Materie zu suchen.“
Anschriften der Verfasser
Dr. med. vet. K.U. Meier
BASF Aktiengesellschaft
67056 Ludwigshafen
Dr. med. vet. R. Reichl
Boehringer Ingelheim Pharma KG
55216 Ingelheim
Literatur:
Bekanntmachung der Neufassung des Tierschutzgesetzes vom 25. Mai 1998
Bundesgesetzblatt 1998, Teil 1, Nr. 30 vom 29. Mai 1998, S. 1105 – 1120
Luepke, N.P.:
The hen’s egg test (HET) – an alternative toxicity test.
Brit. J. Dermat. 115, 133 – 135 (1986)
Schlede, E., Mischke, U., Roll, R., Kayser, D.:
A national validation study of the acute-toxic-class-method – an alternative to the LD50 test.
Arch. Toxicol. 66, 455 – 470 (1992)
Spielmann, H., Berlin:
In-vitro-Methoden (aus Lehrbuch der Toxikologie von H. Marquardt, S.G. Schäfer
BI-Wiss-Verl., 1994
ISBN 3-411-16321-6)
Tierschutzbericht 2001 des BML v.10.04.2001
www.bml.de/tierschutz/tierschutzbericht
Tierschutzbericht der Bundesregierung 1999
Deutscher Bundestag 14. Wahlperiode
Drucksache 14/600 vom 11.03.99
Tierschutzbericht der Bundesregierung 1997
Deutscher Bundestag 13. Wahlperiode
Drucksache 13/7016 vom 27.02.97
York, M., Steiling, W.:
A critical review of the assessment of eye irritation potential using the Draize Rabbit Eye Test.
J. Appl. Toxicol. 18, 233 – 240 (1998)
10 Jahre Zentralstelle zur Erfassung und Bewertung von Ersatz- und Ergänzungsmethoden zum Tierversuch (ZEBET) im BgVV
BgVV Pressedienst vom 21. Juni 1999
Thielallee 88 – 92, 14195 Berlin
